
Hemofilia con inhibidores
El desarrollo de inhibidores en un paciente con hemofilia (hemofilia con inhibidores; HwI) complica el manejo del tratamiento, limitando las opciones del mismo y produciendo resultados deficientes.1 Siempre que se observe una respuesta reducida al tratamiento o niveles de recuperación de factor menores a los previstos en pacientes con hemofilia A (HA) o hemofilia B (HB) que estén expuestos a productos que contienen factores de coagulación, se deberá realizar una prueba para detectar la presencia de un inhibidor.2 El título del inhibidor determinará las opciones de tratamiento para hemorragias agudas y los procedimientos quirúrgicos y odontológicos deben manejarse con cuidado
El diagnóstico preciso de la hemofilia depende de pruebas de coagulación, que se realizan conforme a protocolos y procedimientos rigurosos, y que requieren conocimientos específicos y pericia, así como también el aseguramiento de la calidad.2
Los estudios de la coagulación, incluida la evaluación del tiempo de protrombina (PT) o del tiempo de tromboplastina parcial activada (aPTT), se realizan a cualquier paciente con sospecha de algún trastorno de la coagulación.2 Tanto el PT como el aPTT deben ser normales en pacientes con HA o HB que reciben una terapia de reemplazo adecuada. La aparición repentina de un aPTT prolongado sugiere la presencia de un inhibidor del FVIII o FIX.
Entonces, se requiere una prueba de corrección para confirmar la presencia de un inhibidor si la prueba de corrección no se corrige luego de un tiempo de incubación adecuado.2 Posteriormente, se realiza una prueba de Nijmegen-Bethesda para cuantificar el título del inhibidor.3
Muchos pacientes con inhibidores de baja respuesta (aquellos con un nivel de inhibidor continuamente <5 BU/mL) pueden tratar sus hemorragias y someterse a procedimientos quirúrgicos usando productos de reemplazo de FVIII o FIX.2,4 Es posible que algunos inhibidores de baja respuesta sean transitorios y desaparezcan ≤6 meses después del diagnóstico inicial.2 En el caso de los pacientes con inhibidores de alta respuesta (nivel de inhibidor de ≥5 BU/mL), se utilizan agentes de desvío para controlar los episodios hemorrágicos y durante procedimientos quirúrgicos.2,4
En los pacientes con HwI, los inhibidores son aloanticuerpos que presentan una cinética lineal tipo I, que pueden aumentar o disminuir a lo largo del tiempo.3,5 Algunos inhibidores son transitorios y presentan una remisión espontánea y otros desaparecen en respuesta a la exposición intensiva repetida al FVIII o FIX.6
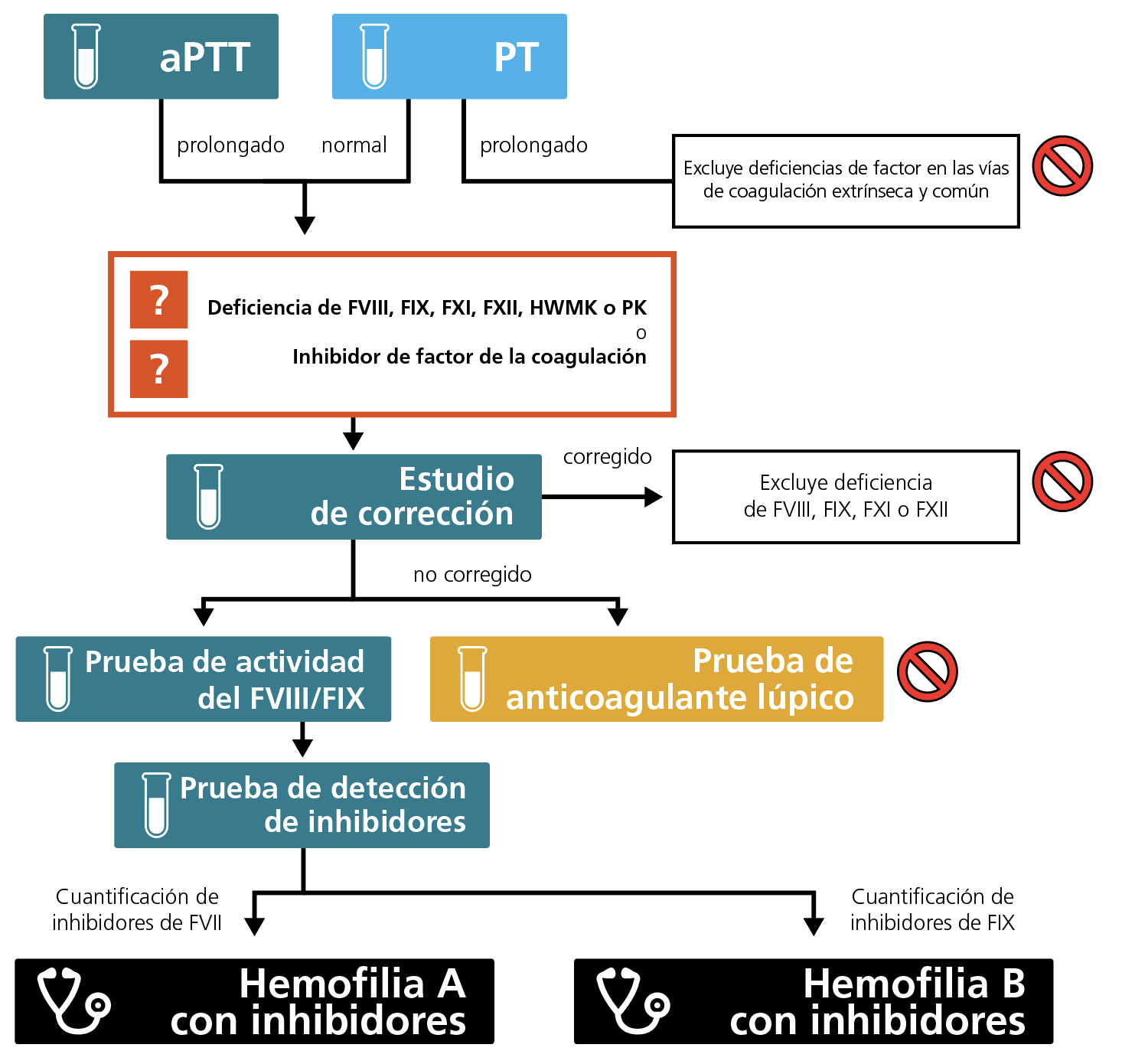
Algoritmo para el diagnóstico en laboratorio de la hemofilia A o B con inhibidores.
Estudios de corrección
Los estudios de corrección se utilizan para confirmar la presencia de un inhibidor. El plasma de prueba se mezcla 1:1 con plasma normal (con 100% de niveles normales de FVIII o FIX) y se incuba a 37 oC durante 1 a 2 horas. Un aPTT prolongado luego de 1 a 2 horas usando una mezcla de plasma normal y plasma del paciente sugiere la presencia de alo o autoanticuerpos; no obstante, se deben realizar las pruebas de coagulación de una etapa y las pruebas cromogénicas de actividad del factor de dos etapas en paralelo
Prueba de Bethesda
La prueba de Bethesda, descrita inicialmente por Kasper y colaboradores en 1975, mide la cantidad de FVIII o FIX inactivo cuando el plasma se incuba con una fuente externa de FVIII o FIX.7 Es posible que esta prueba no detecte los inhibidores de muy baja respuesta.2 La correlación entre el título del autoanticuerpo y los niveles de actividad del FVIII o FIX con la gravedad y el riesgo de hemorragias es muy escasa por lo que las decisiones sobre el tratamiento no deben basarse en los valores de estos análisis de laboratorio.
Prueba de Nijmegen-Bethesda
La prueba de Nijmegen-Bethesda fue desarrollada para mejorar la especificidad y la sensibilidad de la prueba de Bethesda. El título de los aloanticuerpos, que presentan una cinética tipo 1, se cuantifica con la prueba de Nijmegen-Bethesda; no obstante, es posible que el uso de la prueba de Bethesda para cuantificar la cinética no lineal tipo 2 compleja asociada con los autoanticuerpos, y en pacientes con hemofilia adquirida (AHA) no represente de manera precisa la potencia del FVIII.5,7
Diagnóstico diferencial de los inhibidores
Es posible que las pruebas que dependen de fosfolípidos resulten afectadas por la presencia de anticuerpos antifosfolípidos, también conocidos como anticoagulantes lúpicos, que no se dirigen contra ningún factor específico de la coagulación, pero generalmente producen un aPTT, o PT, prolongado en algunos pacientes.8 Estos anticuerpos pertenecen a una familia heterogénea que reacciona con los epítopos de las proteínas en complejos con fosfolípidos de carga negativa.8
Hay varias pruebas específicas disponibles para excluir la presencia de un anticoagulante lúpico, no obstante, se debe realizar más de una prueba ya que no hay ninguna prueba que sea sensible a todos los anticoagulantes lúpicos.9 Las guías de la Asociación Internacional de Trombosis y Hemostasia (ISTH) recomiendan el uso de la prueba del veneno de la víbora de Russell diluido (dRVVT) y una prueba de aPTT con sílice como activador y contenido bajo de fosfolípidos.9 Es necesario realizar pruebas de confirmación con concentraciones crecientes de fosfolípidos con base a las pruebas de detección para verificar la dependencia del anticoagulante lúpico del fosfolípido.9
Pautas internacionales
Las guías de la Federación Mundial de Hemofilia (WFH) recomiendan que se realice una prueba de detección de inhibidores a todos los pacientes que hayan recibido tratamiento intensivo con terapia de reemplazo de factor de coagulación durante >5 días de exposición (EDs), dentro de las 4 semanas de la última infusión.2 Cuando cualquier paciente adulto con >150 días de exposición no responda a la terapia, a la que antes respondía, deberá realizarse una prueba de detección de inhibidores.2 En el caso de pacientes pediátricos con >150 días de exposición a la terapia de reemplazo de factor de coagulación, las pruebas de detección de inhibidores deberán realizarse cada 5 días hasta los 20 ED, cada 10 días hasta los 50 ED, y luego, dos veces al año como mínimo hasta los 150 ED.2 Asimismo, la presencia de inhibidores deberá investigarse previo a una cirugía o si se producen resultados imprevistos en las pruebas de recuperación de factor.
- Berntorp E. Importance of rapid bleeding control in haemophilia complicated by inhibitors. Haemophilia 2011;17:11-6.
- World Federation of Hemophilia (WFH): Guidelines for the Management of Hemophilia; 2012.
- Kasper CK. Diagnosis and management of inhibitors to factors VIII and IX: an introductory discussion for Physicians. World Federation of Hemophilia (WFH) 2004;34:1-26.
- Blanchette VS, Manco-Johnson MJ. Meeting unmet needs in inhibitor patients. Haemophilia 2010;16 Suppl 3:46-51.
- Verbruggen B, van Heerde WL, Laros-van Gorkom BA. Improvements in factor VIII inhibitor detection: From Bethesda to Nijmegen. Semin Thromb Hemost 2009;35:752-9.
- Astermark J. Overview of inhibitors. Semin Hematol 2006;43:S3-7.
- Kasper CK, Aledort L, Aronson D, et al. Proceedings: A more uniform measurement of factor VIII inhibitors. Thromb Diath Haemorrh 1975;34:612.
- Kitchen S, McCraw A, Echenagucia M. Diagnosis of hemophilia and other bleeding disorders. A laboratory manual. Second edition. Montreal, Canada: World Federation of Hemophilia; 2010.
- Pengo V, Tripodi A, Reber G, et al. Update of the guidelines for lupus anticoagulant detection. Subcommittee on Lupus Anticoagulant/Antiphospholipid Antibody of the Scientific and Standardisation Committee of the International Society on Thrombosis and Haemostasis. J Thromb Haemost 2009;7:1737-40.
